据美国食品和药品监督管理局(FDA)官网8月30日(当地时间)消息,诺华公司的CAR-T疗法Kymriah(tisagenlecleucel)正式获批,这也成为全球首个获批的CAR-T疗法。
Kymriah用于治疗3岁-25岁的急性淋巴细胞白血病的复发性或难治性患者。诺华公司是一家总部位于瑞士巴塞尔的制药及生物技术跨国公司。
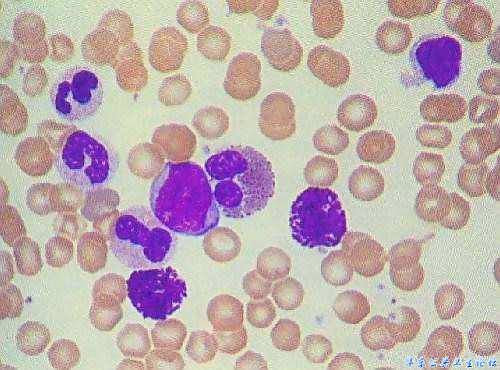
急性淋巴细胞白血病是骨髓和血液中的一种癌症,身体会产生异常的淋巴细胞。该疾病进展迅速,是美国最常见的儿童癌症。国家癌症研究所估计,每年约有3100名20岁及以下的年轻人被诊断为此病。
FDA的官网消息还称,作为一款需要基因改造的自体T细胞免疫疗法,Kymriah疗法的每一次摄入都是针对患者自身T细胞的个性化疗法。
Kymriah从个体患者的体内收集并提取出T细胞,并在生产中心进行遗传改造,使T细胞产生靶向并杀伤带有CD19抗原的白血病细胞。当这些T细胞改造完成后,就会被输注回患者体内,继而杀死癌细胞进行治疗。
Kymriah的安全性与疗效在一个难治性或复发性B细胞前体ALL的儿童和年轻患者多中心的临床试验中得到证实:在治疗的3个月内,CAR-T疗法带来的总体缓解率达到了83%。不过它也可能带来细胞因子风暴和神经系统事件等副作用。“Kymriah是同类首款疗法,填补了罹患这种严重疾病的儿童及青年的重要需求空缺,”FDA生物制品评估和研究中心(CBER)负责人Peter Marks博士说:“Kymriah不仅向这些原本几乎无药可治的患者提供了一种全新的治疗方案,并且该方案在临床试验中体现出了极有希望的缓解和存活率。”
河南省肿瘤医院生物治疗科的主任医师高全立此前接受澎湃新闻采访时解释,“CAR-T借助一款经过改造的T细胞,它比自然状态下的T细胞,杀伤精度更高,能更准确地攻击某种肿瘤细胞,像导弹。CAR是就是人们人为地给这些细胞添加‘瞄准器’。”
T细胞是人体内免疫细胞的一种,是人体抵御病原侵袭的天然防线之一。天然的T细胞是“普通兵种”,而CAR-T相当于“特种兵”。
当遇到特定的肿瘤细胞时,被输入患者体内的CAR-T细胞会被激活,大量增殖,并大开杀戒,攻击和杀死病变的白细胞等肿瘤细胞,达到治疗效果。
Kymriah就是一种CAR-T细胞。
专注肿瘤精准医疗的医药科技公司思路迪的创始人熊磊博士此前曾对澎湃新闻表示,诺华公司在推广应用Kymriah技术时还要解决标准化的难题:如何保证同一家公司在不同区域的实验室,生产出来的细胞,临床能达到一致的治疗水准。
据中国研究型医院学会生物治疗学专业委员会主任委员、解放军总医院生命科学院分子免疫学研究室主任韩为东介绍,尽管Kymriah展现出了惊人的疗效,但其规模生产的稳定性、长期的毒性,以及市场的认可程度等尚需时间检验,还有相当长的一段路要走。
高全立也表示,CAR-T作为前沿技术,目前还不是肿瘤治疗的首选方案,而是推荐应用在传统治疗手段已经无计可施的重症病例上。
而Kymriah此前还遭遇了费用的争议,外界估计患者需要支付数十万美元。
美国一名癌症患者大卫•米切尔(David Mitchell)致信诺华公司首席执行官乔•希门尼斯(Joe Jimenez)称,希望就该公司肿瘤免疫治疗产品Kymriah的公平定价问题,与他会面进行讨论。
诺华公司向澎湃新闻提供的声明称,诺华公司正在慎重考虑Kymriah的合理价格,正在探索基于结果(治疗效果)的定价,这将促进新医疗技术在癌症治疗上的使用。




